若弋生物完成Pre-A+轮数千万人民币融资
近日,苏州若弋生物科技有限公司(下称“若弋生物”)完成了数千万人民币的Pre-A+轮融资,由昆山天使基金投资。本轮融资款将主要用于第三代肉毒素药物管线(Sf9细胞,天然氨基酸序列)的中试至商业化生产工艺的技术转移。此外,昆山还将为若弋生物提供近1万平米的商业化生产车间、相应配套政策及与上海整形医学产业创新研究院合作等产业环境与产业赋能。
元生创投于2022年6月领投若弋生物天使轮融资,并于2023年5月参与其Pre-A轮融资。

若弋生物位于沪昆整形医学及抗衰产业园内的总部及商业化生产车间
核心药物管线——第三代“全天然”重组肉毒素及第四代工程化肉毒素
经过对肉毒素蛋白药物分子机理的深入研究,若弋生物已完成跨越式管线布局,进入了肉毒素药物的3.0和4.0时代。肉毒素第一代产品为其天然宿主肉毒梭菌发酵的蛋白复合物或分离单体,第二代产品为通过基因工程方式引入亲和层析标签和工程蛋白酶酶切位点的重组肉毒素。与第二代产品相比,若弋生物的第三代肉毒素产品不引入任何外源序列,维持了肉毒素100%的天然氨基酸序列(“全天然”),最大限度的保持了与已上市产品可比较的临床确定性,同时通过制剂等方面的优化改善了产品的持续时间、安全窗口、远端扩散性等药物属性;现有2款产品完成终试规模的CMC工艺开发(实验室级别生产流程见企业科研成果 [1] ),进入到IND申报的准备阶段。同时,若弋生物完成了多个工程化改造肉毒素管线(第四代产品)的储备,如基于锌指蛋白递送技术的工程化肉毒素蛋白、AI驱动的肉毒素改造、新血清型重组肉毒素等(详见创始人成果 [2])。
同时,若弋生物完成了多个工程化改造肉毒素管线(第四代产品)的储备,如基于锌指蛋白递送技术的工程化肉毒素蛋白、AI驱动的肉毒素改造、新血清型重组肉毒素等(详见创始人成果 [2])。
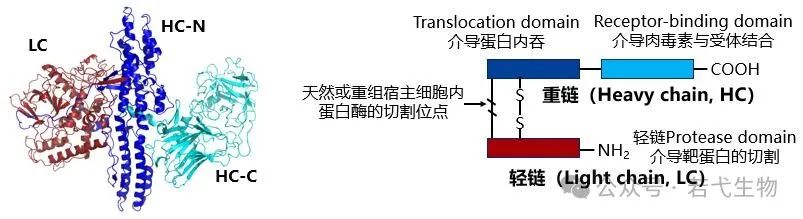
A型肉毒素的三维结构及功能结构域
基于昆虫细胞-杆状病毒合成生物学平台的重组肉毒素制备——摆脱传统细菌生产的生物安全危害
肉毒素第一代产品的肉毒梭菌发酵制备工艺由美国生物化学家、威斯康星-麦迪逊大学教授Edwards Schantz于20世纪60年代在美国特德里克(Fort Detrick)工作期间建立。由于肉毒素蛋白极高的神经毒性和细菌的扩散性,采用肉毒梭菌的生产被认为是存在潜在生物安全危害的(在美国归类为Category A, Tier 1 Select Agent)。近年,随着基因工程技术的发展和大分子药物产业规模的扩大,采用细菌转移性遗传元件(如质粒)进行的重组肉毒素生产逐渐在国内得到了广泛关注。然而,Schantz教授的同事、威斯康星-麦迪逊大学教授Eric Johnson教授的2018年的研究结果表明:细菌中由质粒编码的肉毒素基因会通过水平基因转移(horizontal gene transfer)的方式转移至环境细菌中,造成肉毒素基因的扩散及潜在的生物安全顾虑(参考文献 [3])。
昆虫细胞-杆状病毒系统(Insect cell-baculovirus expression vector system, IC-BEVS)是重组蛋白制剂(特别是多价蛋白疫苗)产业化生产中常用的生产体系;由于杆状病毒在人体不复制、无任何已知相关疾病,一般被认为是较安全的生产体系(见若弋生物研究成果 [4])。更为重要的是,由于昆虫细胞需要特定的温度及培养基、只能在生产车间中存活,因此IC-BEVS体系不会将肉毒素基因扩散至环境中,从而摆脱了肉毒素生产的生物安全问题。同时,若弋生物通过自身研发,完整的解决了IC-BEVS体系的弹状病毒污染和传代稳定性问题(据公开资料,为国内唯一),建立了独立自主知识产权的工艺流程,也因此摆脱了对国外无血清培养基的依赖,实现了发酵工艺的完全国产化,从而解决了商业化生产及产能扩大时的“卡脖子”问题。
昆虫细胞-杆状病毒生产体系






















